Die Skelettmuskulatur
https://www.youtube.com/watch?v=c48KTEuMhAA
Das Gleitfilament der Muskelkontraktion
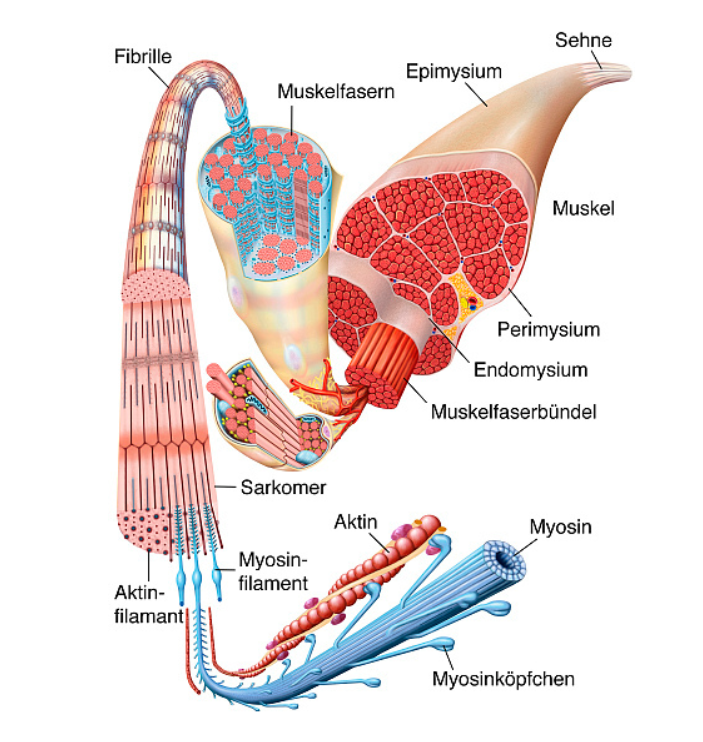
Nach dem Gleitfilamentmodell der Muskelkontraktion verändern weder die dünnen noch die dicken Filamente ihre Länge, wenn sich das Sarkomer verkürzt. Vielmehr gleiten die Filamente längs aneinander vorbei, so dass die dünnen und dicken Filamente stärker überlappen. Das aneinander vorbei gleiten der Filamente basiert auf der Wechselwirkung zwischen Actin- und Myosinmolekülen. Jedes Myosinmolekül besteht aus einer langen Schaftregion und einem Runden seitlich abgeknickten Kopf. Der Schaft aggregiert mit dem Schaft anderer Myosinmoleküle, wodurch das dicke Filament entsteht.
Die Myosinmoleküle im dicken Filament sind bipolar angeordnet, symmetrisch zur M-Linie. Der Kopf ist das Zentrum bioenergischer Reaktionen, die die Muskelkontraktion speisen. Er kann ADP binden und es zu ATP und anorganischem Phosphat hydrolysieren. Die Hydrolyse von ATP wandelt Myosin in eine energiereiche Form um, die an Actin binden und das dünne Filament in Richtung Zentrum des Sarkomers ziehen kann. Die Querbrücke löst sich, wenn ein neues ATP Molekül an den Myosinkopf bindet. In einem sich ständig wiederholenden Zyklus spaltet der freie Kopf das nächste ATP Molekül und heftet sich an eine neue Bindungsstelle auf einem anderen Actinmolekül an, dass näher zur Z-Scheibe auf dem dünnen Filament liegt. Eine typische Muskelfaser in Ruhe enthält ATP für nur einige wenige Kontraktion.
1
https://www.tutory.de/entdecken/dokument/die-skelettmuskulatur-was-staerkt-unseren-koerper
1
https://www.tutory.de/entdecken/dokument/die-skelettmuskulatur-was-staerkt-unseren-koerper


